История человечества знает множество случаев появления в биосфере больших количеств потенциально опасных веществ. Воздействие этих ксенобиотиков (так, напомним, называют вещества, неприемлемые для живых организмов) иногда было причиной трагических последствий, примером которых может служить история с инсектицидом ДДТ. Еще большую печальную известность приобрел диоксин. Долгое время название этого вещества ассоциировалось с Южным Вьетнамом и итальянским городом Севезо, жители которых сполна ощутили насколько смертоносно данное соединение. Но со временем география диоксинов расширилась до размеров всей планеты.
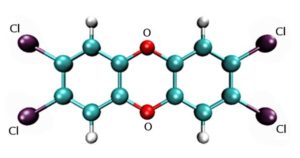
Диоксин, вернее – 2,3,7,8-тетрахлордибензо-пара-диоксин – представляет собой соединение, содержащее два бензольных кольца, в которых по два атома водорода замещено на хлор. Кольца соединены двумя мостиками из атомов кислорода:
Схема образования диоксина при щелочном гидролизе тетрахлорбензола. Эту реакцию обычно проводят в растворе метанола (СН3ОН) под давлением при температуре выше 165оС. Образующийся при атом трихлорфенолят натрия всегда частично превращается в предиоксин, а затем в диоксин. С повышением температуры до 210оС скорость этой побочной реакции резко возрастает, а в более жестких условиях основным продуктом реакции становится диоксин. В этом случае процесс неконтролируем и в производственных условиях завершается взрывом.
Но диоксин является причиной куда более серьезных болезней чем хлоракне. Это начали понимать только после американо-вьетнамской войны. За период с 1961 по 1970 годы американская армия под предлогом борьбы с партизанами распылила на территории Южного Вьетнама 57 тысяч тонн дефолианта «Agent Orange» для уничтожения растительности. Подобные операции пришлось прекратить из-за многочисленных сообщений о раковых и других заболеваниях участников событий, в том числе и военнослужащих США и Австралии, о рождении у них детей-уродов.
Интересно, что сам по себе этот препарат с таким красивым названием (видите, красота опять обманчива) не может вызвать ничего подобного. Но из-за несовершенства его производства упомянутые 57 тысяч тонн дефолианта содержали 170 кг (0,0003 процента!) диоксина, который и наделал столько бед.
Для сравнения отметим, что массовое отравление в итальянском городе Севезо вызвали какие-то несколько килограммов диоксина. При ликвидации последствий этой катастрофы с большой территории пришлось удалять поверхностный слой почвы.
Тем временем в нашей печати, как в научной, так и массовой, до 1985 года диоксинам вообще не было посвящено ни одной публикации. В пятитомной «Краткой химической энциклопедии» (1961 г.) равно как и в изданном значительно позднее «Химическом энциклопедическом словаре» даже слова такого нет! Более того, листая старые подшивки санитарных журналов и сборников, можно найти сообщения о том, что в Уфе с 1964 по 1970 годы работал цех по производству того самого гербицида, который американцы называют «Agent Orange». И 128 человек из 165 обслуживающего персонала заболели неизвестной болезнью, по симптомам совпадающей с хлоракне. Данные эти (без географической привязки) перекочевали в зарубежную печать. А из отечественной прессы они странным (или не очень странным) образом исчезли. Кстати, тот цех реконструировали, потом закрыли. Но что стало с отходами производства — о том молчание. Вы скажете: в те времена иначе и не бывало. Но не повторяем ли мы сегодня ошибки прошлого? Вспомните недавние события в Уфе. Фенолы попали в хлорируемую воду — вот и создались прекрасные условия для образования диоксинов. К тому же они могли сопутствовать фенолам из-за несовершенства технологии производства последних.
ЧТО ИЗВЕСТНО О СВОЙСТВАХ ДИОКСИНА
Строение, физические и химические свойства. Молекула диоксина плоская и отличается высокой симметрией. Распределение электронной плотности в ней таково, что максимум находится в зоне атомов кислорода и хлора, а минимум в центрах бензольных колец. Эти особенности строения и электронного состояния и обусловливают наблюдаемые экстремальные свойства молекулы диоксина.
Диоксин – кристаллическое вещество с высокой температурой плавления (305oС) и очень низкой летучестью, плохо растворяющееся в воде (2×10-8 % при 25oС) и лучше – в органических растворителях. Он отличается высокой термической стабильностью: его разложение отмечается лишь при нагревании выше 750oС, а эффективно осуществляется при 1000oС.
Диоксин – химически инертное вещество. Кислотами и щелочами он не разлагается даже при кипячении. В характерные для ароматических соединений реакции хлорирования и сульфирования он вступает только в очень жестких условиях и в присутствии катализаторов. Замещение атомов хлора молекулы диоксина на другие атомы или группы атомов осуществляется лишь в условиях свободнорадикальных реакций. Некоторые из этих превращений, например взаимодействие с натрий-нафталином и восстановительное дехлорирование при ультрафиолетовом облучении, используются для уничтожения небольших количеств диоксина. При окислении в безводных условиях диоксин легко отдает один электрон и превращается в стабильный катион-радикал, который, однако, легко восстанавливается водой в диоксин с выделением очень активного катион-радикала НО+•. Характерной для диоксина является его способность к образованию прочных комплексов с многими природными и синтетическими полициклическими соединениями.
Токсические свойства. Диоксин – тотальный яд, поскольку даже в относительно малых дозах (концентрациях) он поражает практически все формы живой материи – от бактерий до теплокровных. Токсичность диоксина в случае простейших организмов обусловлена, по-видимому, нарушением функций металлоферментов, с которыми он образует прочные комплексы. Значительно сложнее происходит поражение диоксином высших организмов, особенно теплокровных.
В организме теплокровных диоксин первоначально попадает в жировые ткани, а затем перераспределяется, накапливаясь преимущественно в печени, затем в тимусе и других органах. Его разрушение в организме незначительно: он выводится в основном неизменным, в виде комплексов неустановленной пока природы. Период полувыведения колеблется от нескольких десятков дней (мышь) до года и более (приматы) и обычно возрастает при медленном поступлении в организм. С повышением удерживаемости в организме и избирательного накопления в печени чувствительность особей к диоксину возрастает.
При остром отравлении животных наблюдаются признаки общетоксического действия диоксина: потеря аппетита, физическая и половая слабость, хроническая усталость, депрессия и катастрофическая потеря веса. К летальному исходу он приводит через несколько дней и даже через несколько десятков дней, в зависимости от дозы яда и скорости его поступления в организм.
В нелетальных дозах диоксин вызывает тяжелые специфические заболевания. У высокочувствительных особей первоначально появляется заболевание кожи – хлоракне (поражение сальных желез, сопровождающееся дерматитами и образованием долго незаживающих язв), причем у людей хлоракне может проявляться снова и снова даже через многие годы после излечения. Более сильное поражение диоксином приводит к нарушению обмена порфиринов – важных предшественников гемоглобина и простетических групп железосодержащих ферментов (цитохромов). Порфирия – так называется это заболевание – проявляется в повышенной фоточувствительности кожи: она становится хрупкой, покрывается многочисленными микропузырьками. При хроническом отравлении диоксином развиваются также различные заболевания, связанные с поражениями печени, иммунных систем и центральной нервной системы.
Все эти заболевания проявляются на фоне резкой активации диоксином (в десятки и сотни раз) важного железосодержащего фермента – цитохрома Р-448. Особенно сильно активируется этот фермент в плаценте и в плоде, в связи с чем диоксин даже в ничтожных количествах подавляет жизнеспособность, нарушает процессы формирования и развития нового организма, иными словами, оказывает эмбриотоксическое и тератогенное действие. В ничтожных концентрациях диоксин вызывает генетические изменения в клетках пораженных особей и повышает частоту возникновения опухолей, т. е. обладает мутагенным и канцерогенным действием.
Токсичность диоксина при одноразовом введении
Поведение в окружающей среде. В биосфере диоксин быстро поглощается растениями, сорбируется почвой и различными материалами, где практически не изменяется под влиянием физических, химических и биологических факторов среды. Благодаря способности к образованию комплексов, он прочно связывается с органическими веществами почвы, купируется в остатках погибших почвенных микроорганизмов и омертвевших частях растений. Период полураспада диоксина в природе превышает 10 лет. Таким образом, различные объекты окружающей среды являются надежными хранилищами этого яда.
Дальнейшее поведение диоксина в окружающей среде определяется свойствами объектов, с которыми он связывается. Его вертикальная и горизонтальная миграции в почвах возможны только для ряда тропических районов, где в почвах преобладают водорастворимые органические вещества. В почвах остальных типов, содержащих нерастворимые в воде органические вещества, он прочно связывается в верхних слоях и постепенно накапливается в остатках погибших организмов.
Из почв диоксин выводится преимущественно механическим путем. Отличающиеся низкой плотностью комплексы диоксина с органическими веществами, а также содержащие его остатки погибших организмов выдуваются с поверхности почвы ветром, вымываются дождевыми потоками и в итоге устремляются в низменности и акватории, создавая новые очаги заражения (места скопления дождевой воды, озера, донные отложения рек, каналов, прибрежной зоны морей и океанов).
Проведенные недавно анализы почв некоторых районов Южного Вьетнама указывают на сравнительно небольшое содержание диоксина в поверхностных слоях и на его появление в концентрации до 30 частей на триллион (30 ppt) в глубинных частях почвы. Это свидетельствует о том, что физический и механический перенос в условиях тропиков способствует эффективному рассеянию яда в природе. Однако это не единственный путь миграции диоксина в биосфере. Существует еще перенос этого яда по цепям питания, который способствует его постоянному накоплению в районах максимального потребления зараженных им продуктов питания, т. е. концентрированию в густонаселенных районах.
По мнению вьетнамского ученого и хирурга профессора Тон Тхат Тунга, эффективный биоперенос диоксина в природе способствует постоянному его накоплению теплокровными, причем степень накопления диоксина теплокровными возрастает с увеличением содержания яда в окружающей среде. Это заключение явилось результатом многолетнего изучения последствий прошедшей химичекой войны для обширных контингентов десятимиллионного населения Вьетнама, проживавших и (или) проживающих в районах применения так называемых “безвредных для человека и окружающей среды” гербицидов.
Схема переноса диоксина по цепям питания. Попадая в почву, диоксин поглощается растениями (особенно их подземной частью), почвенной фауной, через которую передается по цепи питания птицам и другим животным. Вынесенный из почв воздушными и водными потоками в акватории, диоксин через зоопланктон, рачков и рыб также попадает к птицам и млекопитающим. Иными словами, с растительной, мясной, молочной (особенно!) и рыбной продукцией, полученной с зараженной территории, диоксин так или иначе попадет на стол к человеку. Высокая стабильность этого яда благоприятствует его многократной циркуляции по цепям питания.











